
「鹽」這個字在最初就是食鹽,我們經常食用的氯化鈉的意思。後來因為化學知識的進步,鹽(salt)這個字被用來代表所有「鹽類」的化合物。酸和鹼反應一定會生成水:
酸+鹼→水+鹽
除了水以外的另一項產品就是鹽。因為有各種不同的酸和鹼所以有各種不同的鹽,但是除了化學方面的書籍以外,鹽這個字通常都是食鹽-氯化鈉的意思。今天我們談的也只是有關食鹽的一些問題。
固體的食鹽是一種由氯離子和鈉離子所構成的結晶,請見圖16-1A。比較大的是氯離子,比較小的是鈉離子,這圖中顯示的是食鹽結晶的一個最基本的單元。這個正立方體的八個角上各有一個氯離子,上下左右前後六個面的中央也各有一個氯離子。鈉離子就在氯離子之間有空的地方,在這正立方體正中心處有一個,在十二個邊的中間也各有一個。許多個這樣的單元疊在一起就成為一個食鹽的結晶,在食鹽的結晶中氯離子和鈉離子是對等的。在圖16-1B中,為了容易看明白,把氯離子和鈉離子都畫得小些,它們的位置也與圖16-1A中的對調了,正立方體的八個角上和六個面的中央各有一個鈉離子,中心處和十二個邊的中央各有一個氯離子,四個圖16-1A的單元,疊在一起,並且把離子都畫得小些,就成為圖16-1C。
在固體食鹽中的每一個氯或鈉的離子雖然並不真的一個個是像彈珠般的小球,像圖16-1A中所畫的那樣,但其相對的位置和距離是大致差不多的。「離子」這個名字取得相當傳神,就像這張圖所顯示的一樣,每一個離子是一個獨立的個體,與相鄰的離子,同類或不同類的,都沒有接觸,是呈分離的狀態。

波爾的的原子模型雖然是過度簡化的模型,但易於解釋許多現象。每一個原子的中心有一個原子核,是由不帶電的中子和帶正電荷的質子構成的。鈉的原子核中有十一個質子,帶十一個正電荷,因此鈉原子核外面的電子軌道上也得有十一個帶負電荷的電子以維持電性的平衡。這十一個電子的分佈是第一層軌道上二個,第二層軌道上八個,第三層軌道上一個。氯的原子核中有十七個帶正電荷的質子,因此,外面的電子軌道上也有十七個帶負電荷的電子。這十七個電子的分佈是第一層軌道上二個,第二層軌道上八個,第三層軌道上七個。每一種原子都有一個傾向,就是希望其最外層的軌道上有八個電子,好像能這樣才最舒服的樣子。鈉原子第二層軌道上有八個電子,如果能把第三層上的那一個借給別人,第二層軌道就成了最外層,上面正好是八個電子。氯原子第三層軌道上有七個電子,如果向別人借一個來,最外層就有八個電子了。鈉原子借了一個電子給別人之後,還剩下十個帶負電荷的電子,比原子核中十一個帶正電荷的質子少了一個,因此成為一個帶有一個正電荷的「鈉離子」。氯原子向別人借來一個電子之後,一共有十八個帶負電荷的電子,比原子核中十七個帶正電荷的質子多了一個,因此成為帶有一個負電荷的「氯離子」。鈉離子和氯離子,一個是借出了一個電子,一個是借來了一個電子,一個帶正電荷,一個帶負電荷,異性相吸,必然是好朋友,但因為二者最外層的電子軌道上都有了八個電子,都感到滿意了,因此不需要結婚,仍然保持著適當的距離,就像圖16-1A中畫的那樣,誰都不記得那一個電子借給誰了或是從那裡借來的。
食鹽-氯化鈉,是一種離子性的化合物,氯與鈉之間好像一群有債權債務關係的異性朋友,其間並沒有婚姻關係。另外有許多有婚姻關係的化合物,一旦接合之後很不容易分開,例如水(一
氧化二氫)就是這樣的化合物,但不在目前討論的範圍之內。固體結晶的食鹽投入於水中,馬上會溶解,成為自由自在的帶一個正電荷的鈉離子和帶一個負電荷的氯離子,每一個鈉或氯離子都是水溶液中獨立的個體。
常有人提出這樣的問題:什麼對人的生命最重要?空氣重要,人若停止呼吸,幾分鐘就會死亡;水重要,人體若不補充水份,幾天就不行了;食鹽也重要,因為人是不能不吃鹽的。人的血漿和組織間的體液中,鹽的濃度大約是百分之一,這是一個相當大的數目。其實有許多元素或離子對人的生命都很重要,例如在肌肉細胞中含量最多的正離子是鉀離子,不是鈉離子,含量最多的負離子是磷酸根離子,不是氯離子。許多元素或離子,在人體中各有其特殊的功能,含量不能過多也不能過少。聽說人體中鋰離子如果含量不足,在精神上會有些不大正常的現象。這些元素或離子都是在日常飲食中攝取的,因此,最好不要偏食。如果某些成份攝取得過多了,健康的人體也有將其排洩掉的機制。
有人說,因為人類是由海洋中的生物進化而來的,血漿和體液中鹽份的濃度和當時海水中鹽份的濃度相當,不知是否正確。海水中的魚類或其他生物的體液中,鹽份的濃度一定要與海水的相等,否則因為滲透壓力的關係很難保持身體內外水份的平衡。
許多社會上的問題,歷史上的大事都與資源的取得或爭奪有關,空氣是維繫生命非常重要的資源,因為隨處皆是,沒有取得的問題,過去也都沒有為了爭奪空氣而引發的鬥爭。但是近年來由於工業的發達,工業的污染成了重要的問題,因為「你污染了我們的空氣」而引發的大大小小的抗爭便時有所聞。水也是維繫生命非常重要的資源,歷史上的幾個重要的文化發祥地都在大河的流域,許多國與國、民族與民族、甚至村落之間的戰爭也都與水源有關。能源也是生活上的重要資源,近年來在中東地區的戰爭,實際上都與油源的爭奪有關。鹽也是每一個人的生活必需品,當然也會引發類似的問題。
動物體內,尤其是血液中,鹽的含量相當高,因此人類在茹毛飲血的狩獵時期,可以從食物中攝取適當的鹽量。但當人類的文明發展到農耕時期,靠穀類及菜蔬維生之後,鹽便成為人生必不可少的食品。因此,人類聚居的地點,除了水源之外必然也與鹽的供應有密切的關係。城鎮、國家的建立與文明的發展都會受到鹽源的影響,許多戰爭也與鹽源的爭奪有關,有的學者認為黃帝與蚩尤之戰的爭端就在於山西解池的鹽源。
因為食鹽是人生的必需品,自然會成為政府專賣抽稅的媒體。鹽稅是自漢朝以來歷代的一項重要稅收,因為專賣抽稅,其生產運銷的制度便非常重要,有制度就有漏洞,要收稅就會有人走私,於是我們在舊小說裡就可以看到一些有關的故事,如鹽梟等等。儒林外史中就有些有錢的鹽商的故事,金瓶梅裡的大惡霸也是一個官鹽的代理商。在民國三十四年時,鹽稅曾高達全國總稅收的52%,俟後由於各方面經濟建設的進步,到了民國六十六年,就是取消鹽稅的那一年,鹽稅已降低到微不足道的全國稅收的0.2%。過去因為鹽務是一種稅務,台灣製鹽總廠是財政部鹽務總局屬下的一個生產單位,到了民國七十年才改隸經濟部的鹽務小組,成為國營事業之一。到了目前,台鹽已經是一個有蓬勃發展前途的多角化經營的「企業公司」。
鹽是一種非常容易溶解在水中的離子性化合物。在地球表面上水的循環系統中,液體水的終點是海洋和許多沒有出口的湖泊。從地面和海上蒸發的水汽在空中冷卻後成為雨或雪降落在地面上,這些天落水在河川流經的途中溶解了可能溶解的土壤中的成份,包括氯離子和鈉離子,河川把所溶解的成份都帶到各自的終點─海洋和沒有出口的湖泊。河川中的水份在到達終點之後是會再蒸發繼續循環的,但是其中所帶的溶質只能聚集起來,因此,海洋的水中便聚集了許多雜質,其中含量最大的成份就是氯離子和鈉離子。在陸地上的那些只有河流注入但沒有水的出口的湖泊便形成鹹水湖,其中含量最大的雜質也是氯離子和鈉離子。這些鹹水湖如果乾涸了就成為表面的鹽礦,若因地殼的變動而埋在地下,便成為地下的鹽礦,可以用鹽井的方式開採。因此,地球表面上水的循環使許多的氯離子和鈉離子聚集在液體水的終點或末端。
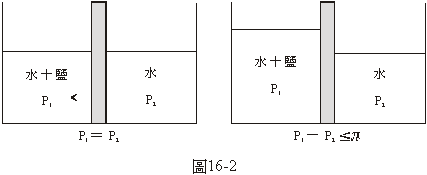
食鹽是一種重要的食物,也是一種重要的工業原料,是大家都知道的,它是製造各種含氯和含鈉化學品的起點。因為食鹽是食物又是離子性化合物,所以是一種非常安全的食物防腐劑。談到食鹽的防腐功能時需要解釋一下滲透現象,如果我們用一片半透膜(水可透過但鹽份不能透過的膜)將一杯水隔成左右兩半(如圖16-2),右邊的一半中放純水,左邊的一半放食鹽水,因為左邊含鹽(氯和鈉離子)的關係,水的濃度降低了,其有效的壓力也打了折扣,使半透膜右方的水的有效壓力比左方高,右方的水便經過半透膜流向左方,一直到平衡為止,這時半透膜兩側的壓力差叫做滲透壓力,
![]() 。
。
這種水份從鹽份濃度低的一側流向濃度高的一側的現象就是所謂的滲透現象。生物的表皮或細胞壁都是可以透過水份的半透膜。每種生物的體液中的電解質都有一定的濃度,如果體外液體中鹽的濃度更高一些的話,體液中的水份就會向外滲透而導致脫水死亡。對於細菌也是一樣,因此,食鹽可以用來殺菌防腐,就像在蛞蝓身上洒一點鹽就會把它殺死一樣。
食鹽以氯離子和鈉離子的形式存在於海水中,其含量雖然依海洋位置的不同有少許的差異,但大約都在3%左右。想像一下,在地球表面上有多少海水,其中的3%是一個非常大的數字。氯離子和鈉離子是獨立地存在於海水中的,因此,海水中氯離子的數目不一定要與鈉離子相等。事實上氯離子要比鈉離子多一點,其比例大約是1:1.18,這是因為海水裡除了氯和鈉之外還有許多其他的離子,重要的帶負電荷的陰離子有硫酸根、碳酸根和溴,重要的帶正電荷的陽離子有鎂、鈣和鉀,連同氯和鈉,總含量大約是海水的3.5%。因為海水的電性是平衡的,所以全部陰離子所帶負電荷的總數和全部陽離子所帶正電荷的總數是一定會相等的。
由以上的資料我們知道,海水當中水約佔96.5%,氯離子和鈉離子約佔3%,其他的離子約佔0.5%。從海水中取鹽可以採取兩種不同策略:其一是把海水中的鹽拿出來;其二是把其中的水拿出去。讓我們先談一下比較舊的第二種策略。把海水中的水拿出去就是要設法使海水蒸發,使海水蒸發需要熱量或是能量,每蒸發1公斤的水份需要539千卡的熱能,而最現成且免費的能量就是太陽能。太陽光一直照射在海面上使海水蒸發,但雨水又一直落回到海面上,落到陸地上的雨水經由河川也會回到大海中,因此,海水的濃度是不會有顯著變化的。蒸發海水製鹽必須在海岸處選擇適當的地點開發為鹽田,其最重要的條件當然是要雨量少、土質適當,使鹽水不致滲漏等等。以鹽田製鹽,數千年來累積了許多經驗,在許多古籍中都有記載。水份的蒸發使海水中離子的濃度逐漸增高,當海水的體積濃縮到原來的一半時,便有微量的氧化鐵和碳酸鈣析出來;濃縮到大約原來的五分之一時,就有一些硫酸鈣析出來;再進一步濃縮到大約原來的十分之一時,氯化鈉的結晶便析出來了;等到大部分的氯化鈉都結晶出來以後,剩下的滷水中還有許多鎂、氯、硫酸根、溴、鉀等的離子,叫做苦滷。
使海水中的水份蒸發當然可以用燒火加熱的方法。我們在地理書上都讀過在四川用天然氣燒火來煮鹽井裡抽出來的鹽水以製鹽的方法,這些方法以現代的眼光看來當然是不經濟的。
在鹽田裡晒出來的或是從鹽礦裡挖出來的食鹽的純度高下不一,視各地的天然條件而定。粗鹽中的雜質不外有以下幾類:(1)夾雜的鹽田中的泥砂,(2)比食鹽溶解度較小的其他鹽類,如前述的硫酸鈣等等,是一些小粒的結晶,(3)一些苦滷附著在食鹽結晶的表面上,(4)食鹽的結晶在生成時不大會把雜質包在結晶的裡面,每一粒結晶都是很純的氯化鈉,但其中或多或少總會有一些雜質。上述的前三種的雜質可以用洗滌的方法除去。用飽和的食鹽水去沖洗,可以把雜質洗掉但不溶解食鹽的結晶。洗過的食鹽再經過乾燥後,純度就相當高了,粉碎後便可以食用。如果純度的要求更高,可以把洗過的食鹽溶解成食鹽水,經過過濾淨化後再蒸發結晶一次。
前面所談的蒸發法,包括日晒和火煮,是把海水中的水拿出去的策略。另外的一個是把海水中的食鹽拿出來的策略。這個策略在離子交換膜研製成功後才得以實現。離子交換膜分為兩種,陰離子膜和陽離子膜。陰離子膜是只有陰離子才可以通過,陽離子不能通過的膜;陽離子膜是只有陽離子才可以通過,陰離子不能通過的膜。圖16-3是一個用電透析的方法濃縮海水的裝置的示
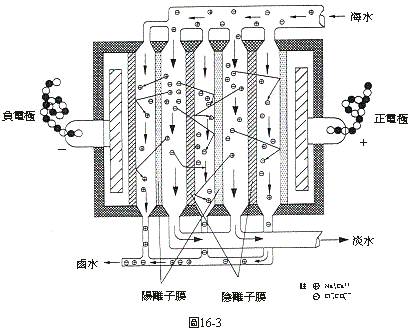
意圖。陰離子膜和陽離子膜交互排列,兩端通以直流電,右方是正電極,左方是負電極。海水自圖的上方進入膜間的每一個間隔,因為通了電流的關係,海水中所有的陰離子都湧向右方的正電極,所有陽離子都湧向左方的負電極。但是因為陽離子只能通過陽離子膜,不能通過陰離子膜;陰離子只能通過陰離子膜不能通過陽離子膜,其結果是在陽離子膜右側陰離子膜左側的間隔中的海水裡,陽離子都透過左邊的陽離子膜跑到左側的間隔中去了,陰離子都透過右側的陰離子膜跑到右側的間隔中去了,陽離子由左邊跑掉了,陰離子由右邊跑掉了,在圖的下端只剩下淡水。在陽離子膜左側陰離子膜右側的間隔中則正相反,陰離子從左邊進來,想從右邊出去但出不去,陽離子從右邊進來,想要從左邊出去也出不去,在這些間隔中,只有離子進來但無法出去,因此而濃縮為濃滷水。濃縮的滷水中鹽的濃度已經很高了,經過少許的蒸發便可以生成食鹽的結晶。
用離子交換膜的電透析法實際上是將電能代替了鹽田上的太陽能,多花了一些電能的成本但省去了鹽灘土地和人工的成本,所得到的精鹽的品質也比較高。目前我們吃的鹽都是台鹽的通宵精鹽廠以電透析法所生產的產品。
世界上有許多地點,對產鹽來說天然的條件太好了,有的是常年雨量非常少的鹽灘,有的是內陸蘊藏豐富的鹽礦,在國際貿易日益開放的大環境中,台灣的鹽業難免會走上進口粗鹽,只從事精製工作的途徑。